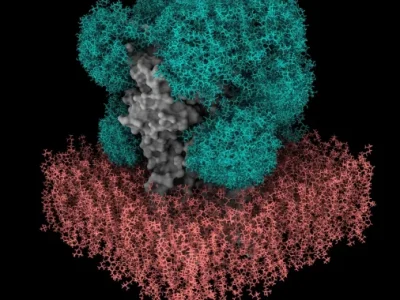
Ein neues Werkzeug der künstlichen Intelligenz kann die Funktionen von Enzymen auf der Grundlage ihrer Aminosäuresequenzen vorhersagen, selbst wenn die Enzyme noch nicht erforscht sind oder nur wenig verstanden werden. Nach Angaben der Forscher übertrifft das KI-Tool mit dem Namen CLEAN die führenden modernen Tools in Bezug auf Genauigkeit, Zuverlässigkeit und Empfindlichkeit. Ein besseres Verständnis von Enzymen und ihren Funktionen wäre ein Segen für die Forschung in den Bereichen Genomik, Chemie, industrielle Werkstoffe, Medizin, Pharmazeutika und mehr.
„So wie ChatGPT Daten aus der geschriebenen Sprache verwendet, um prädiktive Texte zu erstellen, nutzen wir die Sprache der Proteine, um ihre Aktivität vorherzusagen“, sagte Studienleiter Huimin Zhao, Professor für Chemie- und Biomolekulartechnik an der University of Illinois Urbana-Champaign. „Fast jeder Forscher, der mit einer neuen Proteinsequenz arbeitet, möchte sofort wissen, was das Protein tut. Bei der Herstellung von Chemikalien für jede beliebige Anwendung – Biologie, Medizin, Industrie – wird dieses Werkzeug den Forschern helfen, schnell die richtigen Enzyme zu identifizieren, die für die Synthese von Chemikalien und Materialien benötigt werden.
Andere computergestützte Werkzeuge versuchen, die Funktionen von Enzymen vorherzusagen.
Mit den Fortschritten in der Genomik wurden viele Enzyme identifiziert und sequenziert, aber die Wissenschaftler haben nur wenige oder gar keine Informationen darüber, was diese Enzyme tun, sagte Zhao, ein Mitglied des Carl R. Woese Institute for Genomic Biology in Illinois.
Andere computergestützte Werkzeuge versuchen, die Funktionen von Enzymen vorherzusagen. Normalerweise versuchen sie, eine Enzym-Kommissionsnummer zuzuweisen – einen ID-Code, der angibt, welche Art von Reaktion ein Enzym katalysiert -, indem sie eine abgefragte Sequenz mit einem Katalog bekannter Enzyme vergleichen und ähnliche Sequenzen finden. Diese Werkzeuge funktionieren jedoch nicht so gut bei weniger untersuchten oder uncharakterisierten Enzymen oder bei Enzymen, die mehrere Aufgaben erfüllen, sagte Zhao.
„Wir sind nicht die ersten, die KI-Tools zur Vorhersage von Enzym-Kommissionsnummern einsetzen, aber wir sind die ersten, die diesen neuen Deep-Learning-Algorithmus namens kontrastives Lernen zur Vorhersage von Enzymfunktionen verwenden. Wir finden, dass dieser Algorithmus viel besser funktioniert als die KI-Tools, die von anderen verwendet werden“, sagte Zhao. „Wir können nicht garantieren, dass jedes Produkt korrekt vorhergesagt wird, aber wir können eine höhere Genauigkeit erzielen als die anderen zwei oder drei Methoden.“
Die Forscher überprüften ihr Tool experimentell sowohl mit Berechnungen als auch mit In-vitro-Experimenten. Sie fanden heraus, dass das Tool nicht nur die Funktion von zuvor nicht charakterisierten Enzymen vorhersagen konnte, sondern auch Enzyme korrigierte, die von der führenden Software falsch bezeichnet wurden, und Enzyme mit zwei oder mehr Funktionen korrekt identifizierte.
Zhaos Gruppe macht CLEAN online für andere Forscher zugänglich, die ein Enzym charakterisieren oder feststellen wollen, ob ein Enzym eine gewünschte Reaktion katalysieren könnte.
„Wir hoffen, dass dieses Werkzeug von einer breiten Forschungsgemeinschaft genutzt wird“, so Zhao. „Mit der Webschnittstelle können die Forscher einfach die Sequenz in ein Suchfeld eingeben, wie bei einer Suchmaschine, und die Ergebnisse sehen“.
Zhao sagte, die Gruppe plane, die KI hinter CLEAN zu erweitern, um andere Proteine zu charakterisieren, z. B. Bindungsproteine. Das Team hofft auch, die Algorithmen des maschinellen Lernens so weiterzuentwickeln, dass ein Benutzer nach einer gewünschten Reaktion suchen kann und die KI ein geeignetes Enzym für diese Aufgabe findet.
„Es gibt eine Menge uncharakterisierter Bindungsproteine, wie Rezeptoren und Transkriptionsfaktoren. Wir wollen auch ihre Funktionen vorhersagen“, sagte Zhao. „Wir wollen die Funktionen aller Proteine vorhersagen, damit wir alle Proteine einer Zelle kennen und die gesamte Zelle für biotechnologische oder biomedizinische Anwendungen besser studieren oder entwickeln können.“
Die National Science Foundation unterstützte diese Arbeit durch das Molecule Maker Lab Institute, ein von Zhao geleitetes AI Research Institute.