Der menschliche Körper ist in hohem Maße auf elektrische Ladungen angewiesen. Blitzartige Energieimpulse fliegen durch das Gehirn und die Nerven, und die meisten biologischen Prozesse hängen von elektrischen Ionen ab, die durch die Membranen jeder Zelle in unserem Körper wandern.
Diese elektrischen Signale werden zum Teil durch ein Ungleichgewicht der elektrischen Ladungen auf beiden Seiten einer Zellmembran ermöglicht. Bis vor kurzem glaubten die Forscher, dass die Membran ein wesentlicher Bestandteil dieses Ungleichgewichts ist. Dieser Gedanke wurde jedoch auf den Kopf gestellt, als Forscher der Stanford University entdeckten, dass ähnliche ungleiche elektrische Ladungen zwischen Mikrotröpfchen aus Wasser und Luft bestehen können.
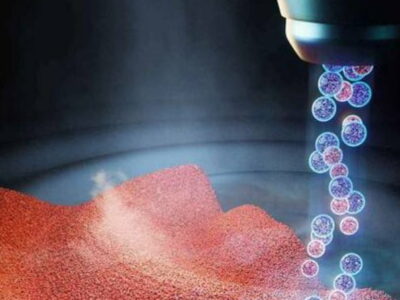
Jetzt haben Forscher der Duke University herausgefunden, dass diese Art von elektrischen Feldern auch in und um eine andere Art von Zellstruktur, die so genannten biologischen Kondensate, existiert. Wie Öltröpfchen, die im Wasser schwimmen, existieren diese Strukturen aufgrund von Dichteunterschieden. Sie bilden Kompartimente innerhalb der Zelle, ohne die physische Begrenzung einer Membran zu benötigen.
Angeregt durch frühere Forschungsarbeiten, die zeigten, dass Mikrotröpfchen aus Wasser, die mit Luft oder festen Oberflächen interagieren, winzige elektrische Ungleichgewichte erzeugen, beschlossen die Forscher zu untersuchen, ob dies auch für kleine biologische Kondensate gilt. Außerdem wollten sie herausfinden, ob diese Ungleichgewichte reaktive Sauerstoff-„Redox“-Reaktionen wie in diesen anderen Systemen auslösen.
Ihre Entdeckung, die am 28. April in der Zeitschrift Chem veröffentlicht wurde, könnte die Art und Weise verändern, wie Forscher über biologische Chemie denken. Sie könnte auch einen Hinweis darauf liefern, wie das erste Leben auf der Erde die für seine Entstehung erforderliche Energie nutzbar machen konnte.
„In einer präbiotischen Umgebung ohne Enzyme, die Reaktionen katalysieren, woher sollte die Energie kommen?“, fragte Yifan Dai, ein Duke-Postdoktorand, der im Labor von Ashutosh Chilkoti, dem Alan L. Kaganov Distinguished Professor für Biomedizinische Technik, und Lingchong You, dem James L. Meriam Distinguished Professor für Biomedizinische Technik, arbeitet.
„Diese Entdeckung liefert eine plausible Erklärung dafür, woher die Reaktionsenergie stammen könnte, genau wie die potenzielle Energie, die einer Punktladung in einem elektrischen Feld verliehen wird“, so Dai.
Wenn elektrische Ladungen zwischen einem Material und einem anderen hin- und herspringen, können sie molekulare Fragmente erzeugen, die sich paaren und Hydroxylradikale bilden können, die die chemische Formel OH haben. Diese können sich dann erneut paaren und Wasserstoffperoxid (H2O2) in winzigen, aber nachweisbaren Mengen bilden.
Zellen können biologische Kondensate bilden, um bestimmte Proteine und Moleküle entweder zu trennen oder zusammenzufassen
„Grenzflächen wurden jedoch nur selten in anderen biologischen Bereichen als der Zellmembran untersucht, die einer der wichtigsten Bestandteile der Biologie ist“, so Dai. „Wir haben uns also gefragt, was an der Grenzfläche biologischer Kondensate passieren könnte, d.h. ob es sich auch um ein asymmetrisches System handelt.“
Zellen können biologische Kondensate bilden, um bestimmte Proteine und Moleküle entweder zu trennen oder zusammenzufassen und so deren Aktivität zu behindern oder zu fördern. Die Forscher beginnen gerade erst zu verstehen, wie Kondensate funktionieren und wofür sie verwendet werden könnten.
Da das Chilkoti-Labor auf die Herstellung synthetischer Versionen natürlich vorkommender biologischer Kondensate spezialisiert ist, war es für die Forscher ein Leichtes, ein Testfeld für ihre Theorie zu schaffen. Nachdem sie die richtige Formel von Bausteinen kombiniert hatten, um winzige Kondensate zu erzeugen, fügten sie mit Hilfe des Postdoktoranden Marco Messina aus der Gruppe von Christopher J. Chang an der University of California – Berkeley dem System einen Farbstoff hinzu, der in Gegenwart von reaktiven Sauerstoffspezies leuchtet.
Ihre Vermutung war richtig. Wenn die Umgebungsbedingungen stimmten, begann an den Rändern der Kondensate ein solides Leuchten, was bestätigte, dass ein bisher unbekanntes Phänomen am Werk war. Als Nächstes sprach Dai mit Richard Zare, dem Marguerite Blake Wilbur Professor für Chemie in Stanford, dessen Gruppe das elektrische Verhalten von Wassertröpfchen untersucht hat. Zare war begeistert, als er von dem neuen Verhalten in biologischen Systemen hörte, und begann, mit der Gruppe an dem zugrunde liegenden Mechanismus zu arbeiten.
„Inspiriert durch frühere Arbeiten über Wassertröpfchen dachten mein Doktorand Christian Chamberlayne und ich, dass dieselben physikalischen Prinzipien gelten und die Redoxchemie fördern könnten, wie z. B. die Bildung von Wasserstoffperoxidmolekülen“, so Zare. „Diese Erkenntnisse legen nahe, warum Kondensate für das Funktionieren von Zellen so wichtig sind.“
„Die meisten bisherigen Arbeiten über biomolekulare Kondensate konzentrierten sich auf ihr Inneres“, sagte Chilkoti. „Yifans Entdeckung, dass biomolekulare Kondensate universell redoxaktiv zu sein scheinen, deutet darauf hin, dass sich Kondensate nicht nur entwickelt haben, um bestimmte biologische Funktionen auszuführen, wie man gemeinhin annimmt, sondern dass sie auch mit einer kritischen chemischen Funktion ausgestattet sind, die für Zellen essentiell ist.“